HAL Allergy und Advanz Pharma starten eine mehrjährige Vertriebspartnerschaft für Deutschland und Österreich. Ziel ist ein besserer Zugang zu modernen, wirtschaftlichen Biosimilars in Dermatologie, Pneumologie und Allergologie. Beide bündelten damit ihre Stärken, um Versorgungslücken zu schließen und biologische Therapien nachhaltiger in der Praxis zu verankern.
ANZEIGE
Die R-Pharm Germany GmbH aus Bayern hat ein vorläufiges Insolvenzverfahren beantragt. Hauptgrund sind Russland-Sanktionen, die Zahlungen und Geschäfte stark beeinträchtigen. Rund 300 Beschäftigte erhielten teils monatelang kein Gehalt. Der Betrieb einer ehemaligen Produktionsstätte von Pfizer im Allgäu läuft eingeschränkt weiter, ein Verwalter prüft Sanierungschancen.
Mitfinanziert durch das österreichische Bundesministerium für Wirtschaft, Energie und Tourismus (BMWET) eröffnet Boehringer Ingelheim Österreich mit der medizinischen Fakultät der Universität Graz ein gemeinsames Forschungslabor im Spezialgebiet des Lungenkrebses.
BIO Deutschland fordert, den geplanten EU Biotech Act entschlossen umzusetzen, um Europas Wettbewerbsfähigkeit zu stärken. Prioritäten sind schnellere Studien, bessere Scale-up-Finanzierung, modernisiertes Beihilferecht und innovationsfreundliche Regulierung. Kritik gibt es am Ausschluss von Novel Food aus Reallaboren – hier sieht der Verband Nachbesserungsbedarf.
Abheben wie ein Kranich, das ist zwar das Firmenmotto der Berliner Kupando, doch im Bereich der Wirkstoffentwickler wird dazu recht profan eine Menge Geld benötigt. Das ist Kupando schon einmal in schwierigen Zeiten 2022 gelungen. In kaum weniger schwierigen Zeiten wurde nun auch ein zusätzlicher Investor und weiteres Geld gefunden, um näher an die klinische Entwicklung herankommen zu können, für einen Ansatz, der das evolutionär ältere Immunsystem aktiviert und in der Breite der Indikationen von Krebs bis hin zu Infektionskrankheiten Einsatzmöglichkeiten verspricht.
Und wieder klingelt die Meilensteinkasse: Evotec erhält von Bristol Myers Squibb 10 Mio. US-Dollar nach dem Start einer Phase I-Studie gegen fortgeschrittenen Nierenkrebs. Der Studienbeginn markiert den ersten klinischen Meilenstein der Protein-Degradation-Partnerschaft. Die Onkologieplattform tritt damit in die Klinik ein und belegt damit das Hamburger Know-how.
Sandoz kooperiert mit Samsung Bioepis bei bis zu fünf Biosimilars. Sandoz erhält exklusive Vermarktungsrechte (außer in Teilen Asiens), Samsung Bioepis übernimmt Entwicklung und Produktion. Die Pipeline könnte auf bis zu 32 Wirkstoffe wachsen und die Marktposition weiter stärken. Sandoz und Samsung entwickeln schon bisher einige gemeinsame Biosimilarprojekte.
Mitte März wurde Felix Winter zum geschäftsführenden Vorstand des Medical Valley EMN e. V. bestellt. Er trat die Nachfolge von Anna Goldsworthy an, die sich neuen beruflichen Herausforderungen widmet.
Formycon und Partner Klinge haben mit Regeneron und Bayer einen Patentstreit um Eylea-Biosimilars beigelegt. Die Vereinbarung ermöglicht den Marktstart von AHZANTIVE und Baiama ab Mai 2026 in Europa sowie weiteren Regionen. Bereits zuvor war der US-Start für Q4 2026 gesichert. Formycon sieht darin einen wichtigen Schritt für den Marktzugang und Wachstum.
Ein Verbund der österreichischen humangenetischen Labore kooperiert mit Golden Helix Inc. (USA), um die genomische Medizin voranzutreiben. Sechs Zentren integrieren NGS-Technologien in standardisierte klinische Abläufe, etwa für Krebs- und Erbkrankheiten. Die mehrjährige Partnerschaft soll damit Diagnostik, Forschung und personalisierte Medizin landesweit stärken.

 peterschreiber.media – stock.adobe.com
peterschreiber.media – stock.adobe.com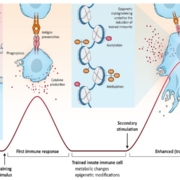 Kupando GmbH
Kupando GmbH Medical Valley EMN e.V.
Medical Valley EMN e.V.